Tofatsitiniibtsitraat on retseptiravim (kaubanimi Xeljanz), mille Pfizer töötas algselt välja suukaudsete Januse kinaasi (JAK) inhibiitorite klassi jaoks. See võib selektiivselt inhibeerida JAK kinaasi, blokeerida JAK/STAT radasid ja seeläbi pärssida raku signaaliülekannet ja sellega seotud geenide ekspressiooni ja aktiveerimist, mida kasutatakse reumatoidartriidi, psoriaatilise artriidi, haavandilise koliidi ja teiste immuunhaiguste raviks.
Ravim sisaldab kolme ravimvormi: tabletid, toimeainet prolongeeritult vabastavad tabletid ja suukaudsed lahused. FDA kiitis selle tabletid esmakordselt heaks 2012. aastal ja toimeainet prolongeeritult vabastav ravimvorm kiitis heaks 2016. aasta veebruaris. See on esimene, mis ravib reumatoidseid liigeseid. Yan on JAK-i inhibiitor, mida võetakse suu kaudu üks kord päevas. 2019. aasta detsembris kiideti taas heaks mõõduka kuni raske aktiivse haavandilise koliidi (UC) uus toimeainet prolongeeritult vabastavate ravimite näidustus. Lisaks on lõppenud praegused naastulise psoriaasi 3. faasi kliinilised uuringud ja käimas on veel kuus 3. faasi kliinilist uuringut, mis hõlmavad aktiivset psoriaatiline artriit, juveniilne idiopaatiline artriit jne. Näidustused. Toimeainet prolongeeritult vabastavate tablettide eelised, mis on pika toimeajaga ja mida tuleb võtta ainult üks kord päevas, aitavad kaasa patsientide haiguste ravile ja kontrollile.
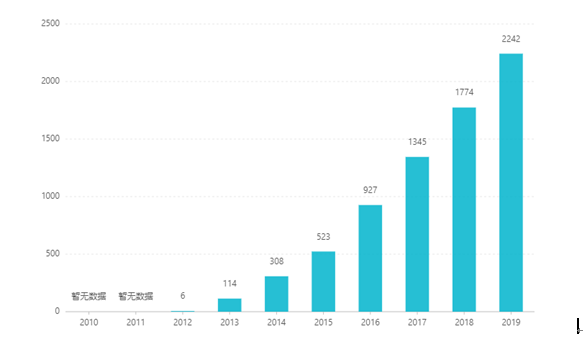
Alates noteerimisest on selle müük aasta-aastalt kasvanud, jõudes 2019. aastal 2,242 miljardi USA dollarini. Hiinas kiideti tablett-annusvorm turustamiseks heaks 2017. aasta märtsis ja 2019. aastal sisenes see läbirääkimiste teel B-kategooria ravikindlustuse kataloogi. Viimane võit pakkumine on 26,79 RMB. Kuid toimeainet püsivalt vabastavate preparaatide kõrgete tehniliste tõkete tõttu ei ole seda ravimvormi veel Hiinas turustatud.
JAK kinaas mängib olulist rolli põletikes ja selle inhibiitorid on näidanud, et nad ravivad teatud põletikulisi ja autoimmuunhaigusi. Seni on ülemaailmselt heaks kiidetud 7 JAK-i inhibiitorit, sealhulgas Leo Pharma delgocitiniib, Celgene fedratiniib, AbbVie upatiniib, Astellase pefitiniib, Eli Lilly baritiniib ja Novartise rokotiniib. Kuid ülalnimetatud ravimite hulgas on Hiinas heaks kiidetud vaid tofatsitiniib, baritiniib ja rokotiniib. Ootame Qilu "Tofatib Citrate Sustained Release Tablets" võimalikult kiiret heakskiitmist ja sellest saavad kasu rohkemad patsiendid.
Hiinas kiitis NMPA 2017. aasta märtsis heaks esialgse uurimistöö tofatsitiibtsitraadi kaubanime Shangjie all ebapiisava efektiivsusega või metotreksaadi talumatusega täiskasvanud RA patsientide raviks. Vastavalt Meineneti andmetele oli tofatsitiibtsitraadi tablettide müük Hiina riiklikes meditsiiniasutustes 2018. aastal 8,34 miljonit jüaani, mis oli palju väiksem kui selle ülemaailmne müük. Suur osa põhjusest on hinnas. Teatatakse, et Shangjie esialgne jaehind oli 2085 jüaani (5mg*28 tabletti) ja igakuine kulu 4170 jüaani, mis pole tavaperedele väike koorem.
Tähelepanu väärib aga see, et tofatsitiib kanti pärast läbirääkimisi 2019. aasta novembris Riikliku ravikindlustusameti poolt 2019. aasta riikliku põhiravikindlustuse, tööõnnetusjuhtumikindlustuse ja rasedus- ja sünnituskindlustuse raviminimekirja. Teatavasti vähendatakse kuutasu alla 2000 jüaani pärast läbirääkimisi hinnaalanduse üle, mis parandab oluliselt ravimi kättesaadavust.
2018. aasta augustis tegi Riigi Intellektuaalomandi Ameti patendi kordusekspertiisikomisjon läbivaatamisotsuse nr 36902 kehtetuks tunnistamise taotluse ja tunnistas spetsifikaadi ebapiisava avalikustamise tõttu kehtetuks Pfizertofatibi põhipatendi, liitpatendi. Pfizertofatiibi kristallivormi patent (ZL02823587.8, CN1325498C, taotlemise kuupäev 2002.11.25) aga aegub 2022. aastal.
Insighti andmebaas näitab, et lisaks esialgsetele uuringutele on kodumaiste tofatsitiniibi tablettidena turustamiseks heaks kiidetud viis Chia Tai Tianqingi, Qilu, Keluni, Jangtse jõe ja Nanjing Chia Tai Tianqingi ravimit. Toimeainet prolongeeritult vabastavate tablettide tüübi kohta esitas Pfizer aga 26. mail turundustaotluse ainult esialgse uuringu põhjal. Qilu on esimene kodumaine ettevõte, kes esitas selle koostise kohta turundustaotluse. Lisaks on CSPC Ouyi BE proovifaasis.
Changzhou Pharmaceutical Factory (CPF) on juhtiv API-de, valmispreparaatide tootja Hiinas, mis asub Jiangsu provintsis Changzhous. CPF asutati 1949. aastal. Oleme pühendunud tofatsitiniibtsitraadile alates 2013. aastast ja juba esitanud DMF-i. Oleme registreerunud paljudes riikides ja saame teid toetada parimate tofatsitiniibtsitraadi dokumentide toega.
Postitusaeg: 23.07.2021